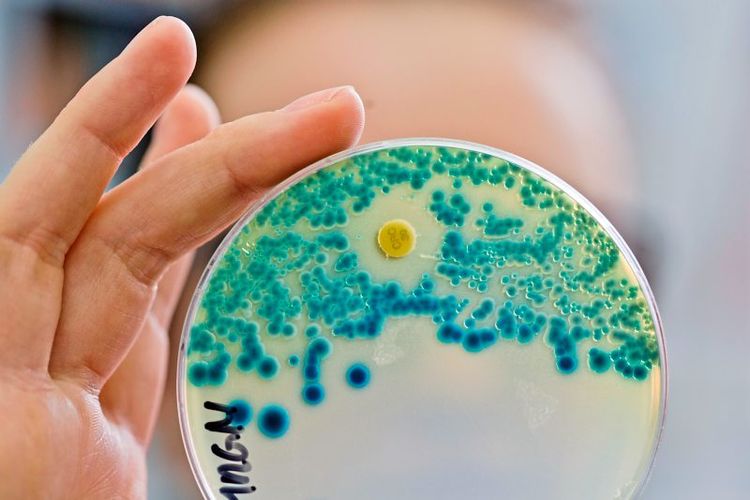
Immer häufiger schlagen Spitäler Alarm, weil antibiotika-resistente Bakterien entdeckt werden. Krankheiten, die früher behandelbar waren, sind es nicht mehr. "Antibiotika-resistente Bakterien sind deshalb so gefährlich, weil sie widerstandsfähig sind – also nur noch schwach oder gar nicht mehr auf herkömmliche Antibiotika reagieren – und darum nur schwer zu behandeln sind", erklärt der Antibiotika-Fachmann Florian Thalhammer, stellvertretender Leiter der Abteilung für Infektionen und Tropenmedizin der Medizinischen Universität Wien.
Bei einigen Bakterien wirken selbst die letzten sogenannten Reserveantibiotika, die Ärzte nur im äußersten Notfall einsetzen, nicht mehr. Und immer mehr Ärzte und Gesundheitspolitiker warnen vor dieser aufkeimenden Gefahr.
Früher galt beispielsweise eine Blasenentzündung als lästig – aber ungefährlich. Selbst wenn sich das Leiden auf das Nierenbecken ausweitete, war das kein Anlass zu großer Sorge. Man konnte die Erreger dann einfach mit einem Antibiotikum unschädlich machen. "Seit einigen Jahren aber treten dabei immer öfter Probleme auf", sagt der Berner Hausarzt Andreas Kronenberg, der das Schweizerische Zentrum für Antibiotikaresistenzen leitet. Denn gegen mehr und mehr Keime können diese Medikamente nichts mehr ausrichten, und sie treiben weiter ihr Unwesen. "Aus einer einfachen Blasenentzündung kann sich eine Blutvergiftung entwickeln, die lebensgefährlich sein kann", so Kronenberg.
Auch in Arztpraxen
Aus Krankenhäusern ist das Problem schon länger bekannt. "Mittlerweile aber stoßen wir auch in Arztpraxen zunehmend auf Bakterien, gegen die einzelne Antibiotika machtlos geworden sind", sagt Kronenberg. Entzündungen, die man jahrzehntelang für bestens beherrschbar hielt, verbreiten wieder Angst und Schrecken. Tritt man zum Beispiel in einen rostigen Nagel und trägt gegen Antibiotika resistente Keime im Körper, kann eine Amputation nötig werden. Und es gibt Fälle, bei denen gar jede Hilfe zu spät kommt:
Experten schätzen, dass solche Keime allein in der Schweiz jedes Jahr mehrere Hundert Menschen töten – etwa gleich viele wie der Straßenverkehr. Manche Ärzte sprechen bereits vom "Anbruch des post-antibiotischen Zeitalters" – der Zeit nach der glorreichen Epoche der Antibiotika-Therapien. Doch ist tatsächlich schon alles verloren?
Ein kurze Geschichte
Der Siegeszug dieser hoch potenten Wirkstoffe begann vor knapp 90 Jahren durch einen Zufall. 1928 experimentierte der schottische Mikrobiologe Alexander Fleming mit sogenannten Staphylokokken. Er bemerkte, dass eine seiner Bakterienkulturen von den Sporen eines Schimmelpilzes befallen worden war – und diese die Staphylokokken zersetzten.
Durch Experimente fand er später heraus, dass Schimmelpilze eine Substanz produzieren, die auch viele weitere Bakterienarten abtötet. Fleming nannte sie "Penicillin". Das Beste: Für Menschen ist diese Substanz, die bei eitrigen Wunden ebenso wirksam ist wie bei Lungen- und Hirnhautentzündungen, ungiftig. Bald darauf wurden weitere Antibiotika entdeckt, und Seuchen wie Pest, Cholera und Tuberkulose konnten weltweit stark zurückgedrängt werden. Doch ab den 1950er Jahren stellten Ärzte fest, dass die vermeintlichen Wundermittel nicht mehr so gut wirkten, wie in der Anfangszeit.
"Bakterien sind Überlebenskünstler", erklärt Florian Thalhammer, stellvertretender Leiter der Abteilung für Infektionen und Tropenmedizin der Medizinischen Universität Wien. "Sie passen sich erstklassig an veränderte Umweltbedingungen an." Manche Keime beginnen beispielsweise, ein Enzym zu produzieren, das die Medikamente zerstört, andere verstärken ihre Hülle und lassen Antibiotika abprallen.
Und das Problem ist hausgemacht: Der Hauptgrund dafür, dass sich immer mehr Resistenzen bilden, liegt darin, dass wir viel zu sorglos mit diesen kostbaren Wirkstoffen umgehen. Wir züchten die widerstandsfähigen Keime also gleichsam selbst. "Ein Paradebeispiel ist die unnötige Therapie mit Antibiotika bei der sogenannten asymptomatischen Bakteriurie, sagt Thalmammer: Vor allem bei älteren Menschen ließen sich häufig Bakterien im Harn nachweisen, ohne dass jedoch eine Infektion vorliege. "Verschreibt man in solchen Fällen als Arzt Antibiotika, so ist das nicht nur völlig übertrieben und sinnlos – sondern grob fahrlässig", so Thalhammer. "Denn die Folgen sind häufig Resistenzbildungen und weitere Kollateralschäden wie starker Durchfall." Dennoch würden manche Hausärzte in Österreich gegen asymptomatische Bakteriurie noch immer solche Präparate empfehlen.
Patienten wollen Antibiotika
Auch Patienten tragen durch ihr Verhalten dazu bei, dass sich ständig weitere Antibiotika-Resistenzen ausbilden. Ausgerechnet ein großer Vorteil der Antibiotika führt sie dabei in Versuchung: Nimmt man solche starke Medikamente ein, lassen die Beschwerden oft schon nach wenigen Stunden nach – und viele Patienten setzen das Präparat gleich wieder ab. Doch mit dem Rückgang der Symptome haben die Antibiotika meist noch nicht alle Krankheitserreger vernichtet, und verbliebene Keime können die Entzündung wieder aufflammen lassen.
Wenn es schlecht läuft, werden sie auch noch widerstandsfähig gegen das Antibiotikum – und vererben die dafür verantwortlichen Resistenz-Gene gar an die Nachkommen, erklärt Thalhammer: "Man sollte Antibiotika schon daher immer genau so lange nehmen, wie es der Arzt vorgeschrieben hat."
Doch selbst manche Mediziner unterschätzen das Problem der Resistenzentwicklung. "Und oft werden Antibiotika in der Tat zu unüberlegt verschrieben", ärgert sich der schweizer Kinderarzt Christoph Berger, Co-Leiter der Abteilung Infektiologie und Spitalhygiene am Universitäts-Kinderspital Zürich. "Bei Schnupfen mit leichtem Fieber etwa sind gerade bei Kindern meist Viren im Spiel, und gegen die können diese Medikamente nichts ausrichten", so Berger. Nur gelegentlich käme es zusätzlich zu einer bakteriellen Infektion. Typisch dafür sei eitriger, gelblich-grüner Schnupfen und hohes Fieber über drei oder mehr Tage. "In über 90 Prozent der Fälle aber sind Erkältungen ohne Antibiotika behandelbar."
Als Alternative empfiehlt Berger, das Fieber zu senken und darauf zu achten, dass der Patient genügend trinke. "Bei verstopfter Nase hat sich der Einsatz von Kochsalzlösung zur Spülung sehr bewährt." Auch Mittelohrentzündungen werden oft von Viren ausgelöst, oder von Bakterien, die nur zu einer leichten Infektion führen und keiner Antibiotika-Therapie bedürfen, sagt er. Es lohne sich, einem Kind, das Ohrenweh hat, Schmerzmittel zu geben und es je nach Alter nach einem oder zwei Tagen erneut zu kontrollieren. "Nur wenn die Zeichen für eine Mittelohrentzündung anhalten, sind Antibiotika nötig." Mit diesem Vorgehen erübrigen sich mehr als 50 Prozent der Antibiotika-Therapien bei Ohrenschmerzen, ohne dass die Patienten deswegen länger Schmerzen oder andere negative Folgen davontragen.
Viren nicht Bakterien
Florian Thalhammer von der Medizinischen Universität Wien ruft ebenfalls zu einem sparsameren Umgang mit Antibiotika auf. "Ein klassisches Negativbeispiel ist der rasant ansteigende Verbrauch solcher Präparate während der kalten Jahreszeit", so der Fachmann für Infektionskrankheiten. "Wenn man sich ansieht, wie häufig Antibiotika während der Erkältungssaison in Österreich verschrieben werden, bekommt man den Eindruck, dass alle Erkrankten eine bakterielle Superinfektion erlitten haben", sagt er und schüttelt den Kopf. "Dabei lassen sich Erkältungsviren mit Antibiotika gar nicht bekämpfen." Denn diese Medikamente wirken ausschließlich gegen Bakterien.
Dennoch sind Antibiotika schwere Geschütze. Sogenannte Breitbandantibiotika etwa greifen alle möglichen Bakterien an: also auch diejenigen, die positive Effekte für unseren Organismus haben. Fast 1000 verschiedene Bakterienarten leben allein im menschlichen Darm. Lakto-Keime, Bifidobakterien und viele weitere Arten tragen zu unserem Wohlbefinden bei und stärken unsere Immunabwehr.
Werden sie vernichtet, kommt kann es oft zu Durchfällen, oder gar zur Ausbreitung gefährlicher Keime. Manche Forscher vermuten, dass wer die Bakterien in seinem Körper mehrfach mit Antibiotika bekämpft, längerfristig seine Anfälligkeit für bestimmte Krankheiten erhöht: Wissenschaftliche Studien zeigen beispielsweise, dass auffallend viele Menschen, die an Asthma oder chronischen Darmentzündungen leiden, als Kind oft mit Antibiotika behandelt wurden.
Supergau durch Ärzte
Warum aber verschreiben Ärzte so häufig solche starke Präparate, selbst wenn es medizinisch nicht nötig oder gar falsch ist? Männer empfehlen schneller Antibiotika als Frauen, hat eine Umfrage unter 3500 Ärztinnen und Ärzten in Deutschland ergeben, und junge Ärzte häufiger als ältere. Als Grund nannten 25 Prozent der Befragten, dass sie "auf der sicheren Seite zu stehen" wollen – also lieber ein zu starkes als ein zu schwaches Medikament verschreiben. 20 Prozent verwiesen darauf, das Patienten schnell genesen und "unbedingt arbeiten wollen". Zwölf Prozent schließlich setzen, nach eigenen Angaben, bereits auf Antibiotika, "wenn der Patient einen langen Anfahrtsweg hatte".
Doch nicht nur in Spitälern und Arztpraxen wird die Entstehung und Verbreitung resistenter Keime gefördert. Auch die Landwirtschaft trägt wesentlich zu diesem Problem bei: Allein in der Schweiz setzen Bauern in der Viehwirtschaft jedes Jahr rund 50 Tonnen Antibiotika ein. Und prompt fand der Basler Kantons-Chemiker Peter Brodmann im Februar 2014 in neun von zehn Hendlfleisch-Proben aus dem Lebensmittelhandel gefährliche, antibiotikaresistente Bakterien.
Antibiotika in der Umwelt
"Geflügelfleisch immer gut durchgaren", rät der Berner Hausarzt und Antibiotika-Experte Andreas Kronenberg. "Dann sterben die Keime ab." Über die Exkremente gelangen resistente Keime aus der Tierzucht aber auch als Dünger auf Äcker und ins Grundwasser. In einem Drittel der Wasserproben aus Flüssen und Seen in der Schweiz wurden resistente Keime gefunden.
Sogar beim Schwimmen in einem Schweizer Badesee kann man sich mit etwas Pech also mittlerweile solche Bakterien einfangen. In Österreich sind bisher keine solchen Daten erhoben worden. Aber auch hierzulande wird sowohl in der Humanmedizin als auch in der Landwirtschaft nicht gerade mit Antibiotika gegeizt. "Obwohl wir da, europaweit gesehen, im besseren Drittel liegen", sagt Thalhammer. Experten wie er gehen dennoch davon aus, dass auch in Österreich Lebensmittel und Umwelt zunehmend mit resistenten Keimen belastet sind. Was also tun?
"Wenn sogenannte Breitbandantibiotika, wie beispielsweise Cephalosporine, künftig weniger häufig und weniger lang eingesetzt würden, wäre schon viel gewonnen", sagt der Zürcher Kinderarzt Christoph Berger. Denn diese Art Antibiotika wirken nicht nur gegen alle möglichen Keime, sondern regen auch alle möglichen Erreger dazu an, sich gegen diesen Angriff zu wehren und Resistenzen auszubilden. Antibiotika wie Penizillin, die spezifischer nur gegen einzelne Bakterienarten wirken, sind daher – wann immer möglich – die bessere Lösung.
Eine Frage der Diagnostik
Selbst für Ärzte ist es allerdings oft schwer abzuschätzen, welche Keimart eine Entzündung ausgelöst hat. Und die mikrobiologische Abklärung der Erreger im Labor dauert mehrere Tage. Forscher des Leibnitz-Instituts für Photonische Technologien in Jena arbeiten daher an einem Laser-Verfahren, um Bakterien schneller zu identifizieren: Trifft Laserlicht auf solche Keime, wird es gestreut – und die Muster, die dabei entstehen, sind so charakteristisch für die unterschiedlichen Bakterienarten, wie beim Menschen der Fingerabdruck. Bald werden Ärzte wohl in weniger als drei Stunden zweifelsfrei eruieren können, welche Keime die Verursacher sind.
Warum aber werden nicht einfach neue Antibiotika entwickelt? "Für die Pharmaindustrie sind diese Medikamente zunehmend ein schlechtes Geschäft", sagt Andreas Kronenberg. Denn viele Erreger finden verblüffend rasch einen Weg, die Attacken durch solche Medikamente zu parieren. Neu entwickelte Antibiotika sind daher oft nur wenige Jahre lang wirksam. Und noch ein Aspekt spielt eine Rolle, weiß Florian Thalhammer von der Medizinischen Universität Wien: Infektionen sind im Regelfall akute Erkrankungen mit einer kurzen Therapiezeit – während chronische Leiden wie etwa Multiple Sklerose oder Alzheimer mit einer lebenslangen Therapiedauer für Pharmakonzerne bessere Gewinnaussichten versprechen.
Neue Ansätze in der Forschung
Inzwischen forschen Pharmakologen aber auch an Medikamenten, die Antibiotika eines Tages ersetzen könnten. Nanowissenschaftler der Universität Bern experimentieren beispielsweise mit winzigen Fettpartikeln, die nicht die Bakterien selbst bekämpfen, sondern ausschließlich deren Gift. "Eine elegante Idee", sagt der Schweizer Hausarzt und Antibiotika-Experte Andreas Kronenberg. Denn bei dieser Methode entstehen keine Resistenzen. Doch zum Jubeln sei es noch zu früh: "Jede Bakterienart produziert unterschiedliche Giftstoffe", so Kronenberg. "Es ist noch keineswegs erwiesen, dass sich die ersten Erfolge ausweiten lassen."
Die Phagentherapie wäre eine interessante Alternative: Bakteriophagen sind Viren, die sich in Bakterien vermehren und dabei ihren Wirt zerstören. Sie greifen jeweils nur eine bestimmte Bakterienart an. Der Therapieansatz wurde bereits 1917 entdeckt und gegen Typhus, Cholera und eitrige Infekte eingesetzt. Doch nach der Entdeckung der Antibiotika geriet er wieder in Vergessenheit. Einzig im früheren Ostblock, wo der Zugang zu Antibiotika schwieriger war, wurde die Phagentherapie weiterhin praktiziert. Mediziner aus Georgien sprechen von einer Erfolgsquote von über 95 Prozent – auch bei antibiotikaresistenten Keimen. Doch nur wenn klinische Studien die Wirksamkeit zweifelsfrei belegen, hat die Methode auch im Westen eine Chance.
Mit vereinten Kräften
Vorerst bleibt also nur der sorgsamere Umgang mit Antibiotika – bei dem Ärzte, Landwirte, Forscher und Patienten gemeinsam gefordert sind. Florian Thalhammer von der Medizinischen Universität Wien schätzt die Chancen, das Problem in den Griff zu kriegen, relativ optimistisch ein:. "Im Rahmen eines Nationalen Aktionsplans zur Antibiotikaresistenz unternimmt das Bundesministerium für Gesundheit in Österreich bereits große Anstrengungen, Ärzte und Patienten weiter für dieses Thema zu sensibilisieren", sagt er.
Und eine Sache macht Experten wie Thalhammer und Kronenberg darüber hinaus Hoffnung: Resistenzen müssen nicht ewig Bestand haben. Für Bakterien bedeutet es oft einen großen Energieaufwand, sich gegen Antibiotika zu wappnen, so Kronenberg. "In einigen Fällen konnte bereits nachgewiesen werden, dass Resistenzraten gegen gewisse Antibiotika, wenn Patienten längere Zeit über keine solchen Medikamente mehr einnahmen, wieder zurückgingen." Die Arzneien zeigten dann plötzlich wieder Wirkung. Vielleicht ist das "antibiotische Zeitalter" also doch noch nicht endgültig vorbei. (Till Hein, 15.10.2016)
Zum Weiterlesen:
Geschlechtskrankheiten: WHO warnt vor Antibiotikaresistenz
EU-Behörde: Reserveantibiotikum Colistin soll reduziert werden